術前診察時に肝機能検査値の異常が見られることがしばしばある。術前評価では、 その異常の原因、重症度、急性障害か慢性障害かを評価し、麻酔のリスクを考えることが重要である。
急性肝障害
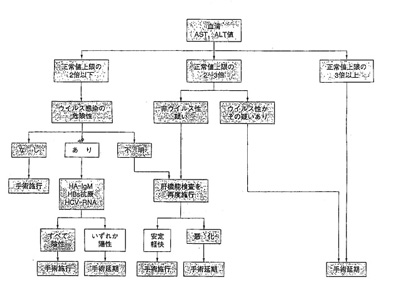
*急性肝障害時の手術の可否を決定するアルゴリズム
特に
①AST、ALTが正常上限値の3倍以下である。
②ウイルス性でない。
③肝機能再検査で安定していること。
が重要である。(Clinical Practice of Anesthesia)
当院の手術適応もほぼ上記のアルゴリズムと同様である。
急性ウイルス性肝炎患者の周術期における重篤な合併症発生率は12%であり、開腹手術後の死亡率は10%である。待機手術であれば、肝機能 検査所見が正常化するまで延期すべきである。
緊急手術が必要な場合は、時間の許す限り検査を行い、肝炎の原因究明と肝機能障害の程度を評価し、電解質の補正、輸液、 原因薬物の除去、凝固因子の補充を行う。
急性肝機能障害時の肝機能検査項目
[代謝機能]
糖負荷試験、血清アンモニア、血清コレステロール
[合成機能]
血清アルブミン値、血清コリンエステラーゼ値、PT、APTT
[排泄機能]
血清ビリルビン値、ICG負荷試験
[肝機能障害]
AST、ALT、ALP、AKBR(動脈血ケトン体比)
B型肝炎患者からの針刺し事故での感染率は30%に達する。
→HBs抗体含有免疫グロブリン(HBIG)とHBワクチンの投与。
C型肝炎患者からの針刺し事故での感染率は3%に達する。
→α-INF(有効性は不明)
薬物性肝障害は薬物あるいはその代謝産物より生ずるが、多剤の相互作用によることもあり、原因薬物の特定はときに困難である。
→原因薬物の中止
薬剤性肝障害を招きやすい薬剤
[中毒性]
アルコール、アセトアミノフェン、サリチル酸、テトラサイクリン、トリクロロエチレン、塩化ビニル、四塩化炭素、黄リン
[特異体質性]
揮発性吸入麻酔薬、フェニトイン、リファンピシン、インドメタシン
[中毒性+特異体質性]
メチルド―パ、イソニアジド、アミオダロン
[胆滞性]
クロルプロマジン、シクロスポリン、経口避妊薬、蛋白同化ステロイド
肝不全時には肝補助療法(CHDFなど)、進行する肝性脳症には肝移植を考慮する。
慢性肝障害
日本におけるB型肝炎ウイルスのキャリアは120万人~140万人、C型肝炎ウイルスの患者は100万人~200万人と推定されている。
症状のない慢性ウイルス性肝炎患者では、術後に肝機能検査値は増悪せず、死亡率も増加しない。術前の肝機能検査値を検討し、
非活動性であると判断されれば、通常の麻酔管理が可能である。
肝硬変による全身の合併症は多臓器にわたる。麻酔管理成功の鍵はこれらの合併症の発生や増悪を予防することである。
肝硬変の合併症
消化管:門脈圧亢進、腹水、食道静脈瘤、痔核、消化管出血
循環:hyperdynamic state、全身性の動静脈シャント
呼吸:肺内シャントの増加、機能的残気量の減少、胸水、拘束性換気障害、呼吸性アルカローシス
腎:二次性アルドステロン症、ナトリウム再吸収の増加
血液凝固:貧血、凝固障害、血小板減少
感染:細菌性腹膜炎
代謝:低Na血症、低K血症、低Mg血症、低アルブミン血症、低血糖
神経:肝性脳症
[肝肺症候群]
肝硬変患者で肺内血管の拡張などにより低酸素脳症をきたすもの。
動脈血酸素分圧が60mmHg未満であれば周術期死亡率が極めて高いため手術適応はない。
[肝腎症候群]
肝不全により腎臓内、特に腎皮質への血流減少によりNa貯留が起こるもの。
プロスタグランジンの代謝異常も関与していると考えられている。
肝硬変患者の予後予測因子としてChild-Pugh分類がよく用いられる。
| 1 | 2 | 3 | |
| 血清ビリルビン | 2.0mg/dl | 2.1~3.0mg/dl | >3.1mg/dl |
| 血清アルブミン | >3.6g/dl | 2.8~3.5g/dl | <2.7g/dl |
| 腹水 | 軽度 | 中等度以上 | |
| 肝性脳症 | 昏迷 | 昏睡 | |
| PT | 4秒以下 | 4~6秒 | 6秒以上 |
肝硬変患者の手術・麻酔によるリスクの検討報告によれば肝硬変患者の周術期死亡率は12%である。周術期合併症発生率は30%で、 最も多い合併症は肺炎である。手術の適応は肝硬変の予後、手術患者の予後、周術期死亡率を考慮して決定しなければならない。
肝硬変患者の周術期死亡危険因子
- ① 男性
- ② Child-Pughスコアが高い
- ③ 腹水がある。
- ④ 原発性胆汁性肝硬変以外の肝硬変
- ⑤ 血清クレアチニン値上昇
- ⑥ 慢性閉塞性肺疾患の合併
- ⑦ 術前の感染症状
- ⑧ 上部消化管出血
- ⑨ 呼吸器系の手術
- ⑩ 術中低酸素の存在
| Child分類 | A | B | C |
| 周術期死亡率 | 10% | 30~31% | 76~82% |
| 非手術患者の死亡率 | 4% | 14% | 51% |
(肝硬変を有する手術患者では非手術患者に比べて死亡率が高い)
(Cf: Child分類 5~6:A 7~9:B 10~15:C)
肝硬変合併肝癌患者に対する肝切除術後の肝不全発症率は術前のⅣ型コラーゲン値とよく相関する。
| 術前Ⅳ型コラーゲン(ng/ml) | <150 | 150~300 | >300 |
| 術後肝不全発症率 (%) | 0 | 11.6 | 44.4 |
(肝線維化の指標であるⅣ型コラーゲン濃度は肝切除術後肝不全発症率に相関する)
術前管理
凝固能異常、腹水、肝性脳症が存在するときは術前に治療が必要とされる。
胆汁鬱滞性疾患においては、凝固能異常はビタミンKの吸収障害によることが多いため、静脈内投与により補正する。
ビタミンKの補充により改善が見られない場合は、新鮮凍結血漿の投与を行い、PT≦3秒となるようコントロールする。
末期の肝硬変患者の血小板減少に関しては、血小板輸血を行い、手術時に10万⁄mm3以上になるよう管理することが推奨されている。
肝性脳症に対しては低吸収性の合成二糖類であるラクツロースやカナマイシンの経口投与などが行われる。
肝腎症候群をきたしている患者は、腹水の補正などにより容易に腎不全に陥るため浸透圧利尿薬や少量のドパミン持続投与により尿量の維持に努める。
急性肝障害患者の麻酔管理
予定手術はできる限り延期する。
急性肝障害患者の高い周術期死亡率は手術および麻酔に伴う総肝血流量の減少に関連していると考えられている。
慢性肝障害患者の麻酔管理
麻酔の導入に主に肝臓で代謝されるプロポフォールやチオペンタールを用いても血流からの薬液の消失は主に再分布によるので影響はない。 単回投与のフェンタニルでは薬物動態に変化は見られないが、持続投与の場合はフェンタニル蓄積の報告がある。将来日本で使用可能になれば、 非特異的なエステラーゼで分解されるレミフェンタニルが用いやすいと考えられる。非脱分極性筋弛緩薬のパンクロニウムは受容体が肝硬変患者 で約50%増加しており、健常人と同等の筋弛緩効果を得るためには初回投与量を増加させる必要がある。パンクロニウムは胆汁排泄率は10%と 低く、主に尿中に排泄される。主に胆汁で排泄されるべクロ二ウム大に用いると性患作用が延長する(0.15mg/kgまでの用量では 薬物動態および作用時間に健常人と比較して差は認められていない。脱分極性の筋弛緩薬のサクシニルコリンは肝臓で産生されるpseudo cholineesteraseに よって分解されるが、慢性肝障害患者でコリンエステラーゼレベルがサクシニルコリンの作用時間を延長させるほど低下していることは稀である。
麻酔の維持に用いる麻酔薬に関して特に制限はないが、ハロタンは肝障害を引き起こしやすいため避けるべきである。 プロポフォールは主に肝臓で代謝されるが、肝外代謝も存在することが示唆されており、プロポフォールを持続投与で肝硬変患者に用いても 半減期に変化はなかったとする報告もある。肝性脳症を呈している患者の場合は、意識障害を遷延させる可能性のある長時間作用性の鎮静薬やオピオイドは避ける。
慢性肝障害患者では大量の腹水が貯留していることが多いが、腹水は血漿と平衡しており、腹水の除去は循環血液量の低下につながる。 したがって、大量の腹水が除去される際には、Na含有量の少ないアルブミン製剤にて補充すべきである。Na含有量の高い輸液にて補充すると 腹水の再貯留を招く。(cf.1lの腹水は約10gの蛋白を含有する。)
麻酔薬の選択
肝循環に対する影響の点から現代の吸入麻酔薬を比較すると、イソフルランの方がセボフルランより肝血流量が維持され、有利であると考えられる。 肝毒性という観点からみるとイソフルランは生体内代謝率が低く、世界的に頻用されている吸入麻酔薬であるので報告数は多い。セボフルランも他の 吸入麻酔薬同様、チトクロームP4502E1 によって代謝されるが、他の吸入麻酔薬と違い肝細胞障害を起こすとされるTFA(塩化トリフルオロ酢酸) 蛋白を生成しない。しかしながら、セボフルランは二酸化炭素吸入装置内のソーダライムと化学反応を起こしコンパウンドAを生成し、これはTFA蛋白 を生成しうることから肝細胞障害を招く可能性を完全には否定できない。統計的に肝硬変を有さない患者の術後肝酵素の上昇をイソフルランと セボフルランで比較した最近の報告では、
両群間に有意差はみられないとするものが多いため、肝毒性に関して同レベルであると考えられている。
導入に使われる静脈麻酔薬としてチオペンタールやチアミラールといったバルビツレート系は、肝疾患患者では低アルブミン血症により 蛋白結合する割合が減少し、活性を有する遊離型の割合が増加するため適宜減量すべきだが、プロポフォールはチトクロムP-450により代謝 されるため半減期は延長するが、クリアランスは影響されないため使用しやすい。
以上の点より、吸入麻酔薬によるものよりTIVAによる麻酔管理を推奨する施設もあるが、 プロポフォールによる脂肪負荷など検討すべき点は多々あり、吸入麻酔による管理より有意に予後を改善するというEvidenceはいまだ示されていない。
硬膜外麻酔
膜麻酔が術後鎮痛の手段として有用であるのは明らかであるが、肝障害患者においては、凝固能障害と血小板数低下から硬膜外血腫の危険性 があり適応には注意を要する。最近の報告では、3区域以上の肝切除患者群でPTの有意な延長と血小板数の有意な低下が術後5日目まで続いたとするものもある。
術後硬膜外鎮痛の薬剤として、モルヒネ単独とモルヒネとロピバカインの併用を比較した研究では、ロピバカインを併用した群が、 腸管機能の回復が有意に早く、術後肺炎の発生も有意に少なかったと報告している。
カテーテルの抜去時期に関する指標は各施設によって異なるが、PT/INR=1.4前後をひとつの目安にするところが多いようである。
出血量・輸血量軽減の工夫
肝切除術においては、常に大量出血の可能性を秘めており、出血に対する対処が術中管理の大きな要点である。
肝切除術の際の出血量を軽減する工夫として、術中の中心静脈圧を低値に保つ方法が報告されている。輸液、輸血の制限、体位の工夫、 ニトログリセリンやニトロプルシドの使用によって肝切除操作中の静脈圧を0~5mmHgにまで低下させ肝切除および止血操作終了後に正常の循環動態に まで循環血液量を回復させる方法で、麻酔管理上hypovolemiaと空気塞栓の可能性をふまえた管理が求められる。この管理法を行う上で留意しなくて はならない点は、静脈圧を低く保つため、突然の大量出血に対する予備力の低下を患者に強いなくてはならないことである。2006年のJAMAで、 術中の静脈圧を低く保つ上記の管理法が予後を低下させるとの報告もあり、どの管理法がよいかというEvidenceはいまだないが、当院の研究で、 現在の手術手技の主流であるPringleの手技によって、虚血再還流後に心筋の拡張障害がおこることが示された。このことを考え合わせると静脈圧を低く 保つという管理法はかなりのhypovolemiaを意味するためhigh riskであるといわざるをえない。また、心臓血管外科手術や肝移植術と同様に線溶系の 阻害剤であるアプロチニンの投与によって輸血量が半減したとする報告もあるが、アプロチニンのアナフィラキシーショックに留意しなくてはならない。
cf. ラジオ波焼却療法
腫瘍中心部に超音波ガイド下に針電極を刺入し、90~100度荷まで熱を加える熱凝固治療法。
全身麻酔下で行われる場合、総エネルギー量に比例した体温上昇が報告されており、注意深い体温管理(冷却)が必要とされる。